|
Význam jódu pre zdravé prsné žľazy
Jód je okrem tvorby tyroxínu esenciálnym, nenahraditeľným elementom podieľajúcim sa na raste a vývoji prsníkov, v dospelosti zohráva kľúčovú úlohu pri kontrole účinkov estrogénov.
Jód pôsobí ako antiproliferatívny prvok zabraňujúci nekontrolovanému deleniu buniek, bráni tvorbe cýst a rakovine, všeobecne chráni funkciu prsnej žľazy viacerými mechanizmami. Najdôležitejším mechanizmom jódu je podpora zachovania schopnosti geneticky naprogramovanbého zániku buniek – apoptózy.
Nedostatok jódu vedie k takzvanému hyperestrogénnemu stavu – nadmerne zosilneným účinkom estrogénov na tkanivá prsnika a vaječníkov s rizikom tvorby cýst a zhubných novotvarov. Deficit jódu môže výrazne zvyšovať riziká vyplývajúce z podávania estrogénov v antikoncepcii. Rovnako deficit jódu vedie k zániku apoptózy a otvoreniu cesty pre nekontrolované delenie buniek.
Vysoký príjem jódu japonskými ženami je spájaný s nízkym výskytom oboch typov – nezhubných a zhubných rakovinových ochorení prsníka. V kontraste uvedeným údajom je preukázaná súvislosť nedostatku jódu a zvýšeného rizika rakoviny prsníka, endometria a vaječníkov. Hypotéza pochádzajúca z roku 1976 vysvetľuje nedostatočný diétny príjem jódu zvýšenou gonadotropnou stimuláciou zapríčiňujúcou hyperestrogénny stav (zvýšenú tvorbu estrónu, estradiolu a znížený pomer tvorby estriolu k estrónu a estradiolu) vyúsťujúci do zvýšeného rizika rakoviny. Uvedenú hypotézu podporuje ďalší fakt, že estradiol zvyšuje proliferáciu – delenie buniek. Novšie vedecké výskumy z roku 2008 zistili že jód potláča rast nádorov cez ovplyvnenie účinkov estrogénov.
Spojitosť rakoviny prsníka ochorením štítnej žľazy bola zistená v štúdii u 26 pacientiek s rakovinou prsníka porovnávajúc so skupinou 22 zdravých žien. Výskyt ochorenia štítnej žľazy bol významne vyšší u žien s ochorením prsníka ako u zdravých žien (58% vs. 18%). Najčastejším syndrómom bol subklinický (bezpríznakový – skrytý) hypotyreoizmus (znížená funkcia štítnej žľazy) u 31% žien s ochorením. Všetky ženy s rakovinou prsníka pochádzali z oblastí s nízkym príjmom jódu. Preto neprekvapuje že nedostatok jódu vedie k zníženej funkcii štítnej žľazy, zníženej antioxidačnej ochrane, zmene aktivity estrogénov a následne k zvýšenému riziku rakoviny prsníka.
Ochranná úloha jódu pred fibrotickým cystickým ochorením prsníka
Benígne, nezhubné fibrocystické ochorenie prsníka (hrčky, cysty v prsníku, fibrocystická mastopátia) je často spájané s nedostatkom jódu.
Experimentálne štúdie na zvieratách zistili že pri zablokovaní vychytávania jódu perchlorátmi nastali tkanivové zmeny so znakmi fibrocystického ochorenia prsnej žľazy, zároveň dochádzalo k vzniku prekanceróznych (predštádium rakovinových) tkanív prsníka. Dvojnásobné riziko fibrocystického ochorenia prsníka bolo zistené u skupiny 90 žien (23 až 50 rokov) so zvýšenými hladinami tyreotropného hormónu (TSH) a zníženou funkciou štítnej žľazy.
V sérii klinických štúdií sa výskumníci zamerali na účinky troch rozdielnych foriem podávania jódu ženám s fibrocystickým ochorením prsníka.
V štúdii 233 dobrovoľníčok dostávalo jodid sodný (KI) počas 2 rokov, skupina 588 žien dostávala jodid viazaný na proteíny počas 5 rokov. 70% žien s podávaním jodidu sodného a 40% žien s podávaním jodidu sodného viazaného na proteíny uvádzali zlepšenie stavu, avšak výskyt nežiadúcich účinkov bol vysoký (sťažené dýchanie, potenie, začervenanie kože).
Podávanie molekulárneho jódu v dávke 3 alebo 6mg/deň 111 ženám s históriou výskytu mastalgie – bolesti prsníka viedlo k významnému zníženiu bolesti, pri podávaní 6mg denne bol zaznamenaný ústup bolesti u 50% pacientiek. V skupine s najnižšou dávkou 1,5 mg/deň nebol v 3 mesiaci podávania zistený významný rozdiel vo výskyte bolesti.
Zdroj: Kessler J.:The effect of supraphysiologic levels of iodine on patients with cyclic mastalgia;Breast J.2004;10
Podľa viacerých zdrojov predstavuje suplementácia – podávanie jódu vysoko účinnú funkčnú výživovú liečbu fibrocystického ochorenia prsníka. Pôsobenie jódu sa vyznačuje synergickým účinkom na viacerých biologických úrovniach súčasne. Molekulárny jód sa javí ako najúčinnejšia forma v liečbe závažných stavov, kde je potrebné podávať relatívne vysoké dávky a dosiahnúť maximálny liečebný efekt, organicky viazaný jód je vhodný na účinnú dlhodobú prevenciu. V porovnaní s jodidmi prináša použitie organicky viazaného a molekulárneho jódu výhodu nižšieho výskytu nežiadúcich účinkov na štítnu žľazu.
Zdroj: Ghent WR.:Iodine replacement in fibrocystic disease of the breast;Can J.Surg.1993;36
Molekulárny jód – forma jódu odporúčaná pri ochoreniach prsníka a vaječníkov
Molekulárny jód (I2) je účinnejšou formou podávania jódu v liečbe fibrocystického ochorenia a rakoviny prsníka v porovnaní s anorganickými soľami jódu. Tkanivo prsníka v období, keď nevytvára materské mlieko, vykazuje nízku aktivitu enzýmu – peroxidáza. Počas neprodukčného štádia dochádza znížením aktivity enzýmu k zníženej schopnosti premieňať anorganické formy jódu (napríklad jodidovaná soľ, doplnky výživy s anorganickými soľami jódu) na organické.
Použitie molekulárneho jódu umožňuje dosiahnúť vyššie tkanivové koncentrácie jódu bez účasti enzýmu peroxidáza, v konečnom dôsledku vedie k zvýšenej tvorbe jódolaktónov blokujúcich tvorbu cýst.
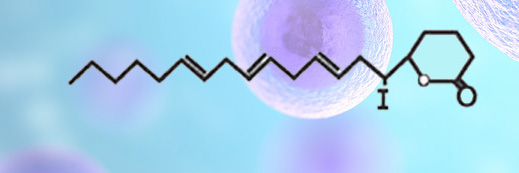
obrázok: delta-jódolaktón – molekula zabezpečujúca obmedzenie tvorby cýst
In vitro štúdie (experimentálne) preukázali že molekulárny jód potláča delenie rakovinových buniek a navodzuje apoptózu – programovaný zánik bunky pri viacerých typoch buniek rakoviny prsníka. Podávanie I2 potláčalo rozvoj oboch typov rakovinových novotvarov, nezhubných aj zhubných.
Molekulárny jód umožňuje dosiahnúť vyššie koncentrácie jódu na povrchu buniek a tým umožniť vytváranie jódolaktónov. Bunkové steny obsahujú značné množstvá kyseliny arachidónovej s ktorou vytvárajú jódolaktóny. V experimentoch sa zistilo že rakovinové bunky obsahujú až dvojnásobne vyššie koncentrácie kyseliny aracchidónovej, cieľovej molekuly pre molekulárny jód.
Rakovinové bunky majú pre vyšší obsah kyseliny arachidónovej selektívne vyššiu schopnosť absorbovať jód a vytvárať jodolaktóny. Zvýšená tvorba jodolaktónov odvodených od kyseliny arachidónovej (IL-6) aktivuje uzavretie bunkového cyklu a navodzuje programový zánik bunky – apoptózu. Pochopenie uvedeného mechanizmu vysvetľuje protirakovinové účinky molekulárneho jódu a úspešné klinické výsledky.
Podľa výsledkov ďaľších štúdií anorganické formy jódu vo forme solí (napríklad jodid draselný, KI) nemajú antiproliferatívne = protirakovinové účinky.
Organicky viazaný jód a elementárny – molekulárny jód vykazujú výrazné antiproliferatívne účinky obmedzujúce tvorbu cýst prostredníctvom zvýšenia tvorby jódolaktónov.
|
- Nutraceutiká vo výžive
- Omega3
- Cievne choroby
- Mastné kyseliny
- Účinky
- Imunitný systém
- Alergia
- Astma
- Suchá pokožka
- Nervové choroby
- Očné choroby
- Ženské choroby
- Rizikové tehotenstvo
- Dávkovanie omega-3 počas tehotenstva
- Dojčiace matky
- Starnutie
- Rakovina tlmenie rastu nádorov
- Rakovina omega-3 zvyšuje účinnosť chemoterapie
- Metabolizmus
- Obsah v potravinách
- Ideálne zastúpenie
- Ľanový alebo prírodný rybí olej?
- Optimálny príjem
- Záver
- Čierne korenie
- Enzýmy
- Gurmar
- Horká tekvička
- Chlorella
- Jód
- Karnozín
- Koenzým Q10
- Kokosový olej
- Konopný olej
- Kurkuma
- Kyselina alfa-lipoová
- Mladý jačmeň
- Nikotínamid mononukleotid
- Stévia
- Škorica
- Tekvicový olej
- Vitamín A
- Vitamín D
- Vitamín E
- Zázvor
- Zelený čaj
- Železo
- Omega3
- Nutraceutiká a ochorenia
- Alergia
- Bolesť chrbtice
- Cukrovka
- GcMAF imunoterapia
- Epilepsia
- Hypertrofia prostaty
- Chrípka
- Mozog a nootropiká
- Nízkosacharidová diéta
- Očkovanie prevencia reakcií
- Očné choroby
- Oslabená imunita
- Opar na perách
- Oslabený rast vlasov
- Raynaudov syndróm
- Reumatoidná artritída
- Srdcovo cievne choroby
- Vysoký krvný tlak
- Žilová trombóza
- Produkty
- Všetky produkty
- Omega-3 rybí olej natural
- Rybí olej s vitamínom D
- Rybí olej s organicky viazaným jódom
- Rybí olej s koenzýmom Q10
- Horká tekvička čaj
- VerbePLX kapsuly
- Gurmar antidiabetický čaj
- Karnozín
- Nikotínamid mononukleotid
- Turmerix – kurkumové kapsle
- OraMAF suspenzia
- Prírodný vitamín E
- Serapeptáza
- Blog
- Rybí olej – užívanie
- Kontakt
- Nutraceutiká vo výžive
- Omega3
- Cievne choroby
- Mastné kyseliny
- Účinky
- Imunitný systém
- Alergia
- Astma
- Suchá pokožka
- Nervové choroby
- Očné choroby
- Ženské choroby
- Rizikové tehotenstvo
- Dávkovanie omega-3 počas tehotenstva
- Dojčiace matky
- Starnutie
- Rakovina tlmenie rastu nádorov
- Rakovina omega-3 zvyšuje účinnosť chemoterapie
- Metabolizmus
- Obsah v potravinách
- Ideálne zastúpenie
- Ľanový alebo prírodný rybí olej?
- Optimálny príjem
- Záver
- Čierne korenie
- Enzýmy
- Gurmar
- Horká tekvička
- Chlorella
- Jód
- Karnozín
- Koenzým Q10
- Kokosový olej
- Konopný olej
- Kurkuma
- Kyselina alfa-lipoová
- Mladý jačmeň
- Nikotínamid mononukleotid
- Stévia
- Škorica
- Tekvicový olej
- Vitamín A
- Vitamín D
- Vitamín E
- Zázvor
- Zelený čaj
- Železo
- Omega3
- Nutraceutiká a ochorenia
- Alergia
- Bolesť chrbtice
- Cukrovka
- GcMAF imunoterapia
- Epilepsia
- Hypertrofia prostaty
- Chrípka
- Mozog a nootropiká
- Nízkosacharidová diéta
- Očkovanie prevencia reakcií
- Očné choroby
- Oslabená imunita
- Opar na perách
- Oslabený rast vlasov
- Raynaudov syndróm
- Reumatoidná artritída
- Srdcovo cievne choroby
- Vysoký krvný tlak
- Žilová trombóza
- Produkty
- Všetky produkty
- Omega-3 rybí olej natural
- Rybí olej s vitamínom D
- Rybí olej s organicky viazaným jódom
- Rybí olej s koenzýmom Q10
- Horká tekvička čaj
- VerbePLX kapsuly
- Gurmar antidiabetický čaj
- Karnozín
- Nikotínamid mononukleotid
- Turmerix – kurkumové kapsle
- OraMAF suspenzia
- Prírodný vitamín E
- Serapeptáza
- Blog
- Rybí olej – užívanie
- Kontakt
Fibrocystické ochorenie prsníka
You are here:
- Home
- Nutraceutiká vo výžive
- Jód
- Fibrocystické ochorenie prsníka

